Vamos contar tudo o que precisas saber sobre o aminoácido essencial L-Fenilalanina.
Índice
O que é a L-fenilalanina
A L-fenilalanina é um aminoácido, ou seja, um elemento constituinte das proteínas.
A nível funcional é um nutriente essencial, um aminoácido indispensável, já que o nosso organismo não possui a capacidade de sintetizar de forma endógena.
É por isso pelo que requeremos do seu consumo a través da dieta ou outra via de administração externa para não sofrer caquexia.
Figura I. Representação gráfica de um processo caquexico.
Deficit de fenilalanina
Sofrer caquexia por uma insuficiência de L-fenilalanina exclusivamente é práticamente impossível e nunca foi reportado na literatura científica só nos casos de pacientes com nutrição parenteral em ausência deste aminoácido.
A caquexia, acontece no geral com a mau-nutrição proteica, por consumos pobres de proteínas em geral e não tanto por um aminoácido.
Embora, a fenilalanina não somente é um aminoácido essencial para a síntese de proteínas, já que no organismo cumpre uma função importante endocrina na síntese de catecolaminas; e as características da sua estrutura química que outorgam uma peculiaridade muito interessante aos outros aminoácidos.
Onde posso encontrar fenilalanina
A L-fenilalanina está presente em práticamente qualquer fonte de proteínas alimentares:
- Carnes (vaca, galinhas, porco).
- Peixes.
- Leite e derivados lácteos.
- Ovos.
- Produtos de soja (proteínas, farinhas e tofu).
- Certos frutos secos possuem pequenas concentrações.
Aspartamo e fenilalanina
Algo interessante é que uma fonte dietética de L-fenilalanina é o aspartamo.
Obviamente, de forma mais significativa em sociedades desenvolvidas e industriais (especialmente Estados Unidos, onde o consumo de aspartamo é muito alto).
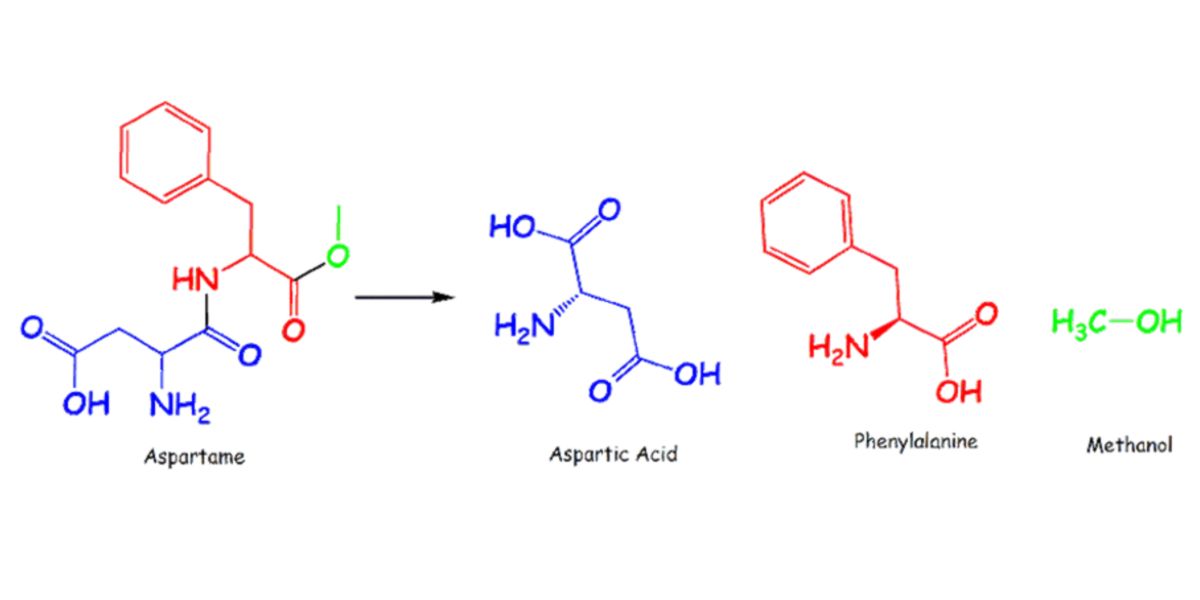
Figura II. Divisão da estrutura química do aspartamo, um dipéptido metil éster.
Ainda assim, um adulto médio ingere aproximadamente 5g de L-fenilalanina ao dia quando a ingesta dietética recomendada em base a uma dieta isoenergética para um homem média é 8g ao dia (HDMB, s.f.)
A pesar da grande presença da fenilalanina em alimentos do uso comum, aparece que a nossa ingesta não chega a ser suficiente acorde as proporções de aminoácidos estabelecidas.
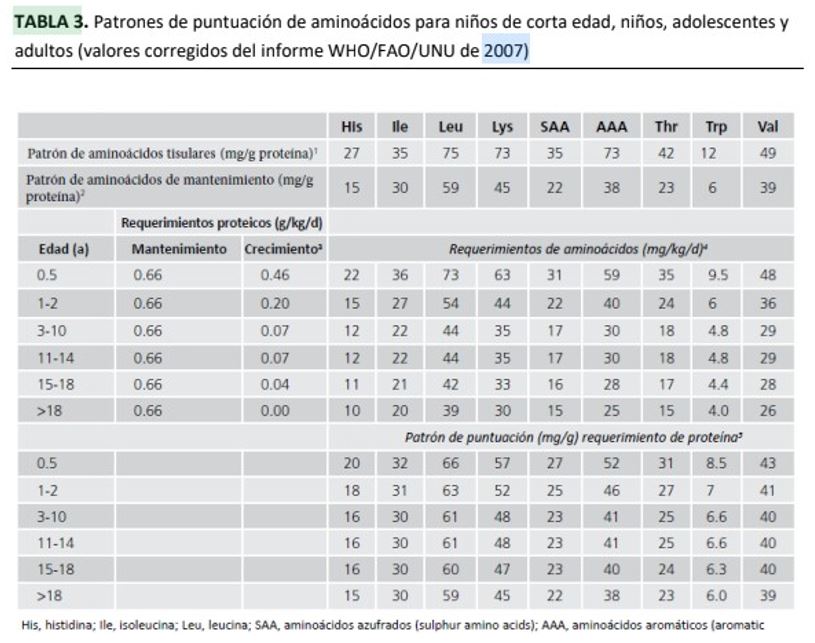
Figura III. Recomendações do consumo de aminoácidos (g/kg/dia) em função da idade.
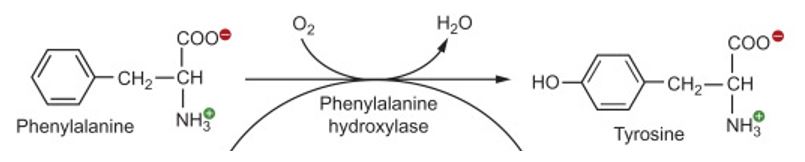
Figura IV. Representação gráfica do processo de conversão (hidroxilação) da L-fenilalanina a L-tirosina.
Para que serve a L-fenilalanina
Síntese de proteínas musculares
Qualquer aminoácido que pertence ao grupo dos aminoácidos proteinogénicos que codificam o nosso genoma pode e será utilizado para sintetizar proteínas nos tecidos do organismo, incluindo o tecido muscular.

Figura V. Representação gráfica de 20, dos actualmente proposto 22, aminoácidos proteinogénicos.
Deles, os aminoácidos essenciais são especialmente sensíveis para este processo.
Já que o resto pode ser sintetizados a partir destes, más os aminoácidos essenciais não podem ser criados “de novo”.
Pelo que aqui não há tutelagem, ou se administram de fora ou se mantemos ao longo prazo um consumo deficitário de algum deles sofreremos um processo catabólico para obter a partir das nossas proteínas.
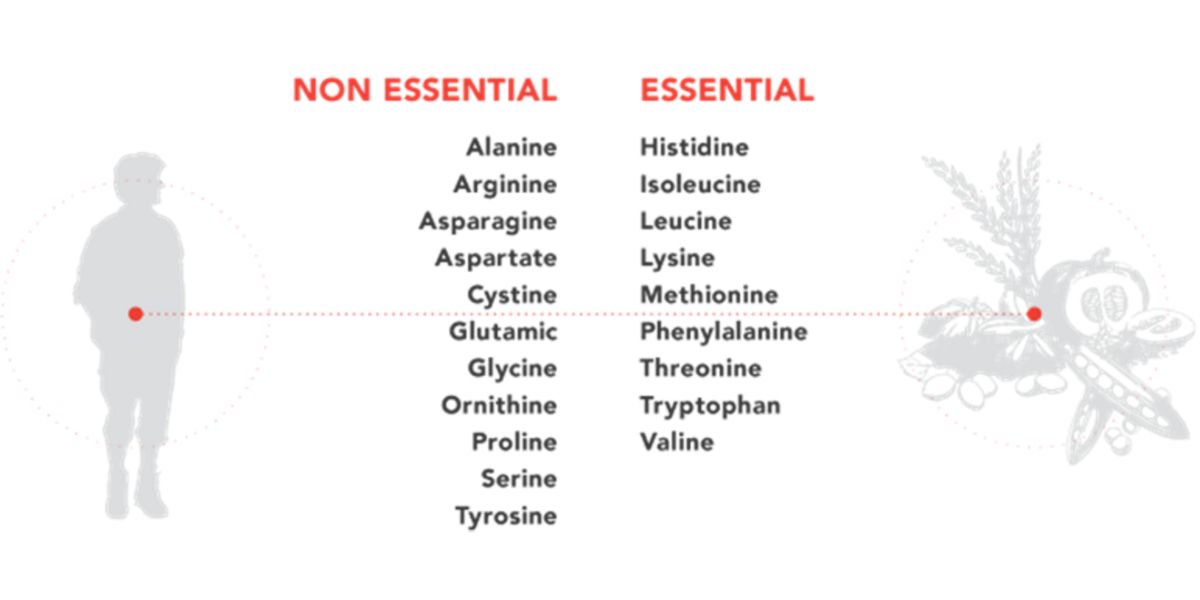
Figura VI. Representação gráfica da categorização funcional dos aminoácidos em essenciais/não essenciais.
É por isso que certificam o consumo dos aminoácidos essenciais é essencial e, a tabela anterior que anexei as quantidades recomendadas destes aminoácidos, não estaria mal revisar a tua dieta para ver si estás bem cobertos.
Síntese de catecolaminas
A L-fenilalanina é o aminoácido que inicia o processo de síntese de catecolaminas.
Sendo estritamente académicos, o aminoácido que começa é a L-tirosina, más como a fenilalanina se converte em tirosina que podemos falar que está é realmente o “primeiro passo funcional”.
Este processo acontece no fígado, a través da ação da enzima fenilalanina hidroxilasa.
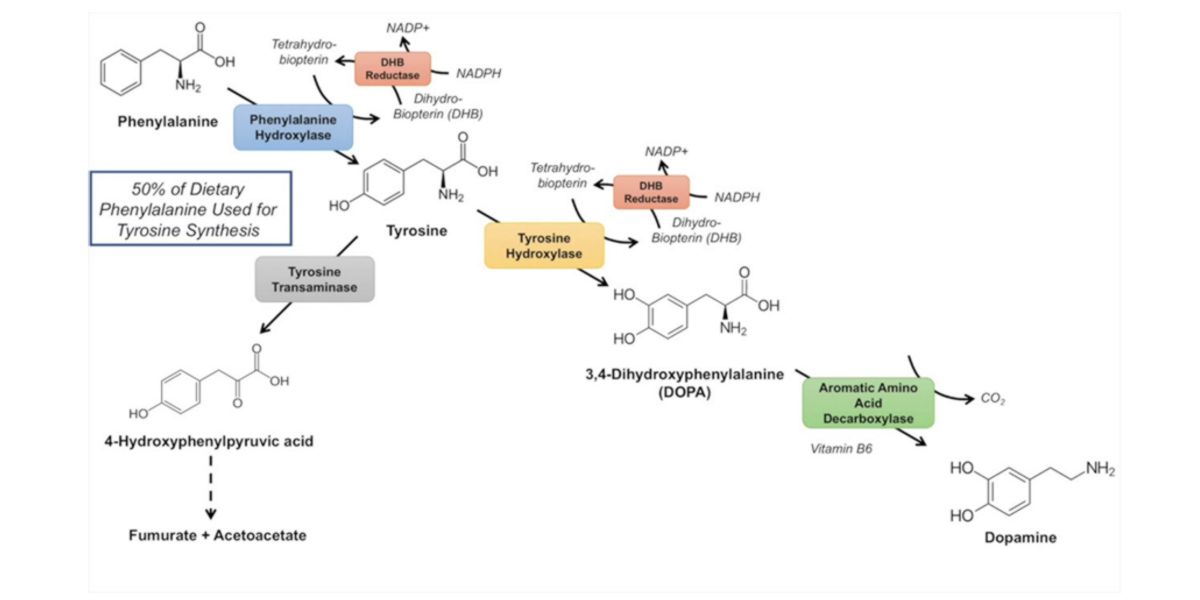
Figura VII. Processo de síntese das catecolaminas.
A partir daí, a tirosina dirige-se neuronas dopaminérgicas e noradrenérgicas do sistema nervoso central, aos nervos simpáticos e aos feocromocitos da médula adrenal e aos paraganglios na periferia para sintetizar L-dopa, e está ao mesmo tempo continua para gerar a dopamina e ao mesmo tempo a sua vez epinefrina e norepinefrina.
Todo este processo tem importantes implicações neurometabólicas, específicas a cada hormona que foi sintetizada, ou seja, a dopamina tem um rol no sistema límbico e outras estruturas tanto corticais como extracorticais sobre a regulação das emoções.
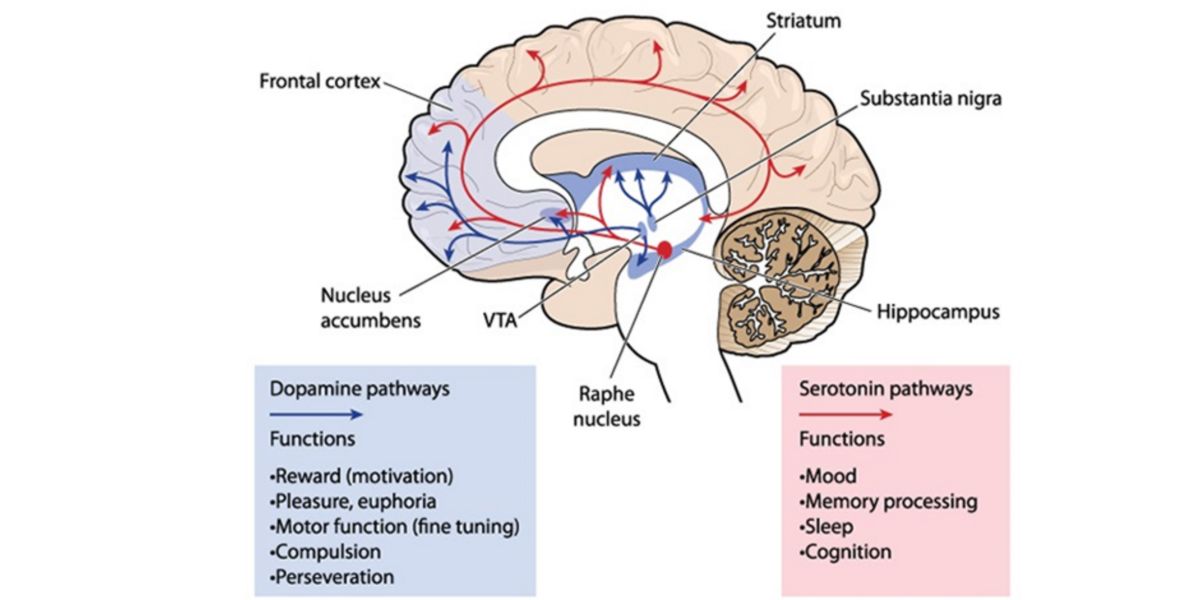
Figura VIII. Representação gráfica simplificada do mecanismo de produção da dopamina e a serotonina e os seus efeitos centrais.
Enquanto as funções das adrenalina e a noradrenalina estão mais caracterizadas pelo seu perfil estimulante do sistema nervoso simpático, mediadas pelos receptores adrenérgicos que modulam a contração/relaxamento do músculo liso, aumentam a lipólise, activam no sistema RAAs, etc.

Figura IX. Principais efeitos do agonismo a receptores alfa e beta adrenérgicos em diferentes tecidos.
Esta é a razão pela que a L-fenilalanina tem um papel importante sobre os processos como a lipólise (primeiro passo da “queima de gorduras”); a partir dela, se sintetizam as hormonas responsáveis deste efeito.
A evidência é um pouco conflitiva, especialmente porque devemos ter em conta que a enzima limitante da síntese de catecolaminas é a tirosina hidroxilasa, e que ao consumir um precursos, sua actividade não será afectada.
Ainda assim, intervenções como as de Ueda et al. (2017) mostram um aumento agudo das concentrações de glicerol no plasma, uma amostra de hidrólise dos triglicéridos intracelulares do lipid droplet dos adipocitos, e por tanto da lipólise.
Regulação da saciedade
Talvez a propriedade mais curiosa e destacado deste aminoácido:
A fenilalanina é um nutriente altamente saciante.
Isto se deve a influência que possui sobre a secreção de colecistoquinina (CKK), uma hormona peptídica que é produzida no duodeno e regula certos processos da digestão, entre eles a regulação da velocidade do vaziado gástrico.
Graças a este efeito, a colecistoquinina foi proposta como um potente supressor do apetite (Johnson, 2013); a autêntica hormona que antagoniza a acção da ghrelina mais que a leptina realmente pelos seus mecanismos.
A colecistoquinina secreta nas alterações mecânicas do volume gástrico, ou seja, é a que nos da a sensação de saciedade quando estamos “cheios” mesmo que seja só de alface, comparte mecanismo com o PYY.
Além disso, a secreção do colecistoquinina é tremendamente sensível as concentrações de ácidos gordos e aminoácidos presentes na quimo quando passa pelo intestino.
Os aminoácidos aromáticos (como a fenilalanina, a tirosina, ou o triptófano) sãos os mais efectivos para aumentar a secreção da CKK (Liddle, 1994).
A fenilalanina parece ser o mais potente de todos embora não conhecemos com precisão dos seus mecanismos.
Demonstrou modular as concentrações intracelulares de cálcio nos enterocitos de modelos animais, e o que é mais importante, demonstrou em humanos no desenvolvimento exercer um efeito anorexígeno.
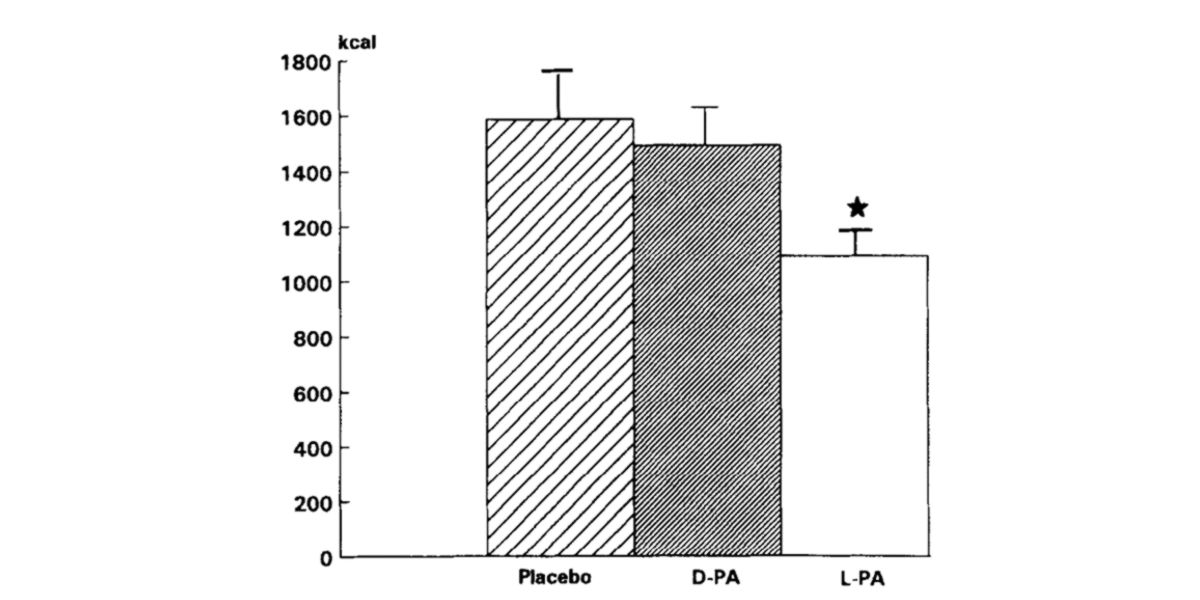
Figura X. Efeitos sobre o consumo calórico após o consumo da L-fenilalanina (L-PA), D-fenilalanina (D-PA) e Placebo numa intervenção ad libitum.
O grupo que consumiu L-fenilalanina antes da refeição sentiu saciado muito antes que o grupo que consumiu D-fenilalanina o placebo e, por tanto, a sua ingesta energética foi muito menor.
Este efeito foi conseguido graças as mudanças na secreção de CKK no grupo L-fenilalanina, embora, e contra a lógica, o grupo que usou D-fenilalanina não sofreu as mesmas mudanças
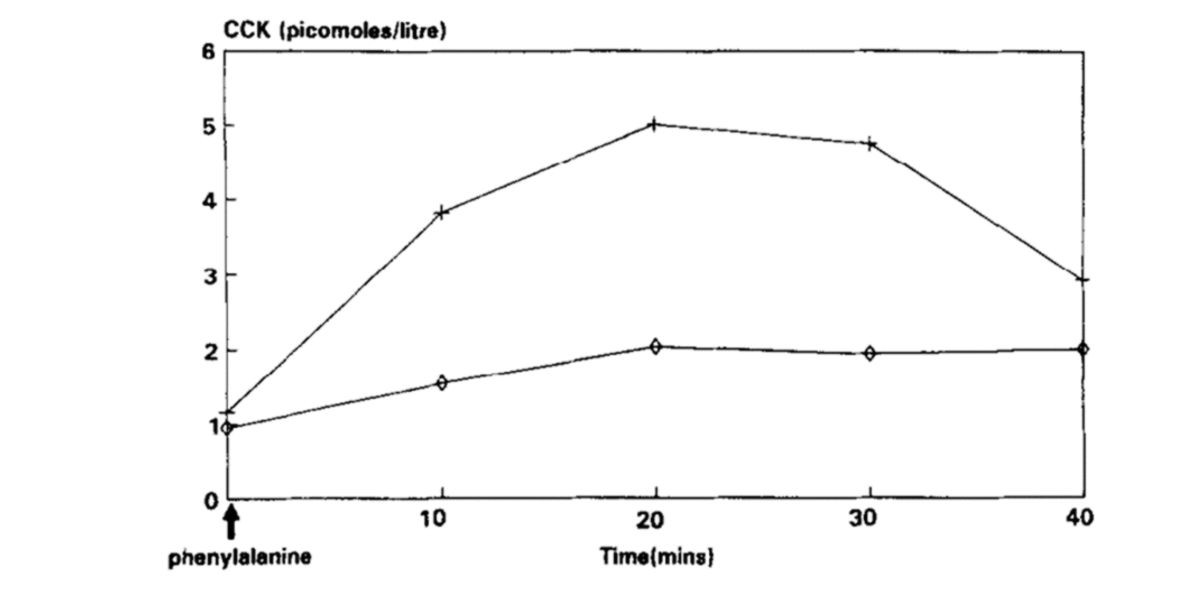
Figura XI. Curva de secreção de CKK após a administração da L-fenilalanina (cruzes) e D-fenilalanina (rombos).
Como já sabemos de algum tempo, a quiralidade e a configuração estereoisomérica dos aminoácidos que influi no seu mecanismo de ação, farmacocinética e farmacodinamia.
L-Fenilalanina da HSN
Na HSN realizamos um screening da literatura científica sobre o uso da L-fenilalanina e consideramos que é um nutriente que está suficientemente caracterizado e conta com uma forte evidencia em humanos.
Seguindo a nossa filosofia tradicional da gama RawSeries, um produto de máxima pureza, sem aditivos que alteram o conteúdo do suplemento alimentar.
100% Vegan
Na lista de ingredientes da nossa fenilalanina encontrarás:
L-fenilalanina (produzido a través de um processo de fermentação vegetal). E nada mais!
A denominação do “produzido a través de um processo de fermentação vegetal” se deve que a nossa crença de que os suplementos nutricionais devem ser acessíveis para o mundo independentemente da sua condição ou posição ao respeito ao consumo de qualquer tipo de alimento.
Por isso encontraras isto nos nossos produtos:

Figura XII. “A destacar” na HSN, ausência de alergénios e aptitude em dietas vegetarianas e veganas.
Que indica:
Ausência de alergénios
Que sempre trabalhamos para seleccionar as matérias primas de máxima qualidade, e formular produtos livres destes compostos.
Produto apto para vegetarianos e veganos
Desde alguns meses rejeitamos os aminoácidos derivados de fontes animais, e unicamente utilizamos matérias-primas sem uso dos mesmos, na sua maioria, procedentes de fontes vegetais como o milho.
Máxima pureza de origem vegetal! O que mais precisas?
Fontes Bibliográficas
- Ballinger, A. B., & Clark, M. L. (1994). l-Phenylalanine releases cholecystokinin (CCK) and is associated with reduced food intake in humans: Evidence for a physiological role of CCK in control of eating. Metabolism, 43(6), 735–738.
- EFSA Panel on Dietetic Products, N. and A. (NDA). (2010). Scientific Opinion on the substantiation of health claims related to L phenylalanine and increased alertness (ID 708, 1629), enhancement of mood (ID 657), pain relief (ID 657) and improvement of memory (ID 658) pursuant to Article 13(1) of Regulation (EC) No 1924/2006. EFSA Journal, 8(10), 1748.
- Konturek, S. J., Radecki, T., Thor, P., & Dembinski, A. (1973). Release of Cholecystokinin by Amino Acids. Proceedings of the Society for Experimental Biology and Medicine, 143(2), 305–309.
- Matthews, D. E. (2007). An Overview of Phenylalanine and Tyrosine Kinetics in Humans. The Journal of Nutrition, 137(6), 1549S-1555S.
- National Center for Biotechnology Information. PubChem Database. Phenylalanine, CID=6140.
- National Center for Biotechnology Information. PubChem Database. Cholecystokinin, CID=16129670.
- Pacak, K., Timmers, H. J. L. M., & Eisenhofer, G. (2015). Pheochromocytoma. In J. L. Jameson, L. J. De Groot, D. M. de Kretser, L. C. Giudice, A. B. Grossman, S. Melmed, … G. C. B. T.-E. A. and P. (Seventh E. Weir (Eds.), Endocrinology: Adult and Pediatric (Vol. 2–2, pp. 1902-1930.e6).
- Pohle-Krauza, R. J., Navia, J. L., Madore, E. Y. M., Nyrop, J. E., & Pelkman, C. L. (2008). Effects of l-phenylalanine on energy intake in overweight and obese women: Interactions with dietary restraint status. Appetite, 51(1), 111–119.
- Wang, Y., Chandra, R., Samsa, L. A., Gooch, B., Fee, B. E., Michael Cook, J., … Liddle, R. A. (2011). Amino acids stimulate cholecystokinin release through the Ca2+-sensing receptor. American Journal of Physiology – Gastrointestinal and Liver Physiology, 300(4), G528-37.




 Blog de Fitness, Nutrição, Saúde e Desporto | Blog HSN En el Blog de HSNstore encontrarás tips sobre Fitness, deporte en general, nutrición y salud – HSNstore.com
Blog de Fitness, Nutrição, Saúde e Desporto | Blog HSN En el Blog de HSNstore encontrarás tips sobre Fitness, deporte en general, nutrición y salud – HSNstore.com 





